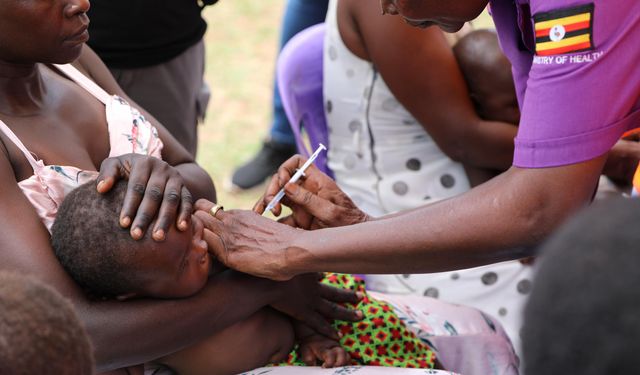
BEİJİNG, 8 Nisan (Xinhua) -- Westlake Yaşam Bilimleri ve Biyotıp Laboratuvarı'ndan araştırmacılar, mikropların tümör hücrelerini ele geçirebildiğini ve bu konak hücrelerin kan dolaşımındaki mekanik strese karşı gücünü artırabileceğini buldu.
Laboratuvarda çalışan makalenin kıdemli yazarı Cai Shang, "Araştırmamız, kanser hücrelerinin davranışının aynı zamanda tümörlerin içinde saklanan mikroplar tarafından da kontrol edildiğini ortaya koyuyor. İlk başta bunların çoğunun steril olduğu düşünülüyordu" dedi.
Cai ve birlikte çalıştığı meslektaşları, hücrelerinde belirgin miktarlarda canlı bakteri bulunan, insanlardakine benzer meme kanserinin fare modelini kullandı. Cell dergisinde Perşembe günü yayımlanan araştırmaya göre, kanser dokusundaki bakteriler, normal meme dokusundakinden yaklaşık 10 kat daha zengin.
Araştırmacılar, mikropların kanser hücreleriyle birlikte dolaşım sisteminde dolaşabildiğini ve bu yolcu bakterilerin, kasların kasılmasını da içeren birçok çeşit hücre hareketine katılan bir protein olan hücresel aktin ağını düzenleyebildiğini buldu.
Araştırma, bu mikropların kanseri yerinde etkilemek yerine kanser hücrelerinin yer değiştirmesinde uzmanlaştığını da gösterdi. Cai, "Meme tümörüne sadece tek bir doz bakteri enjekte edilmesi bile normalde nadiren metastaz yapan bir tümörün metastaz yapmaya başlamasına sebep olabilir" diye konuştu.
Araştırmacılar, bulguların ardından özellikle tümör bakterilerini ortadan kaldırmak için farenin kanına antibiyotik enjekte etti ve tümörün küçülmediğini ancak akciğerdeki metastazın belirgin şekilde azaldığını buldular.
Araştırmaya göre, mikropların tekrardan fareye enjekte edilmesi de metastazı belirgin şekilde artırdı. Araştırmacılar, konuyu, kandaki tümör hücrelerinin "akış kesme basıncı" adı verilen mekanik gerilim altında ölme eğilimi göstermesi ancak içlerindeki mikropların iskeletlerini yeniden inşa ederek onları daha güçlü yapması şeklinde açıklamaya çalıştı.
Araştırmada, bakterilerin böylesine olumlu bir mutualizm (karşılıklı fayda hali) yaratmak için tümör hücrelerini nasıl istila edip gelişmeyi başardığı açıklanmadı. Araştırmacılar, daha derinlikli bir çalışmanın, kanser ilaçlarının klinik kullanımında antibiyotiklerin uygun şekilde uygulanmasına dair yeni bir strateji için ipucu verebileceğini söyledi.
Cai, bulguların, an itibariyle antibiyotiklerin kanser tedavisi sırasında kullanımının hastalara fayda sağlayacağını kanıtlamadığını söyledi.